5月6日國(guó)家藥品監(jiān)督管理局官網(wǎng)發(fā)布《國(guó)家藥監(jiān)局綜合司關(guān)于印發(fā)2019年國(guó)家醫(yī)療器械抽檢產(chǎn)品檢驗(yàn)方案的通知》(下稱《通知》),向各省����、自治區(qū)、直轄市藥品監(jiān)督管理局印發(fā)2019年國(guó)家醫(yī)療器械抽檢產(chǎn)品檢驗(yàn)方案���。
意味著����,根據(jù)此前國(guó)家藥監(jiān)局印發(fā)的《國(guó)家藥監(jiān)局關(guān)于開展2019年國(guó)家醫(yī)療器械抽檢工作的通知》要求�����,2019醫(yī)療器械抽檢工作全面啟動(dòng)��。
國(guó)家藥監(jiān)局近日發(fā)通知���,全國(guó)醫(yī)療器械抽檢工作啟動(dòng)�,抽檢方案印發(fā)���。
5月6日���,國(guó)家藥品監(jiān)督管理局官網(wǎng)發(fā)布《國(guó)家藥監(jiān)局綜合司關(guān)于印發(fā)2019年國(guó)家醫(yī)療器械抽檢產(chǎn)品檢驗(yàn)方案的通知》(下稱《通知》),向各省�、自治區(qū)、直轄市藥品監(jiān)督管理局印發(fā)2019年國(guó)家醫(yī)療器械抽檢產(chǎn)品檢驗(yàn)方案�。
這意味著,根據(jù)此前國(guó)家藥監(jiān)局印發(fā)的《國(guó)家藥監(jiān)局關(guān)于開展2019年國(guó)家醫(yī)療器械抽檢工作的通知》要求��,2019醫(yī)療器械抽檢工作全面啟動(dòng)���。
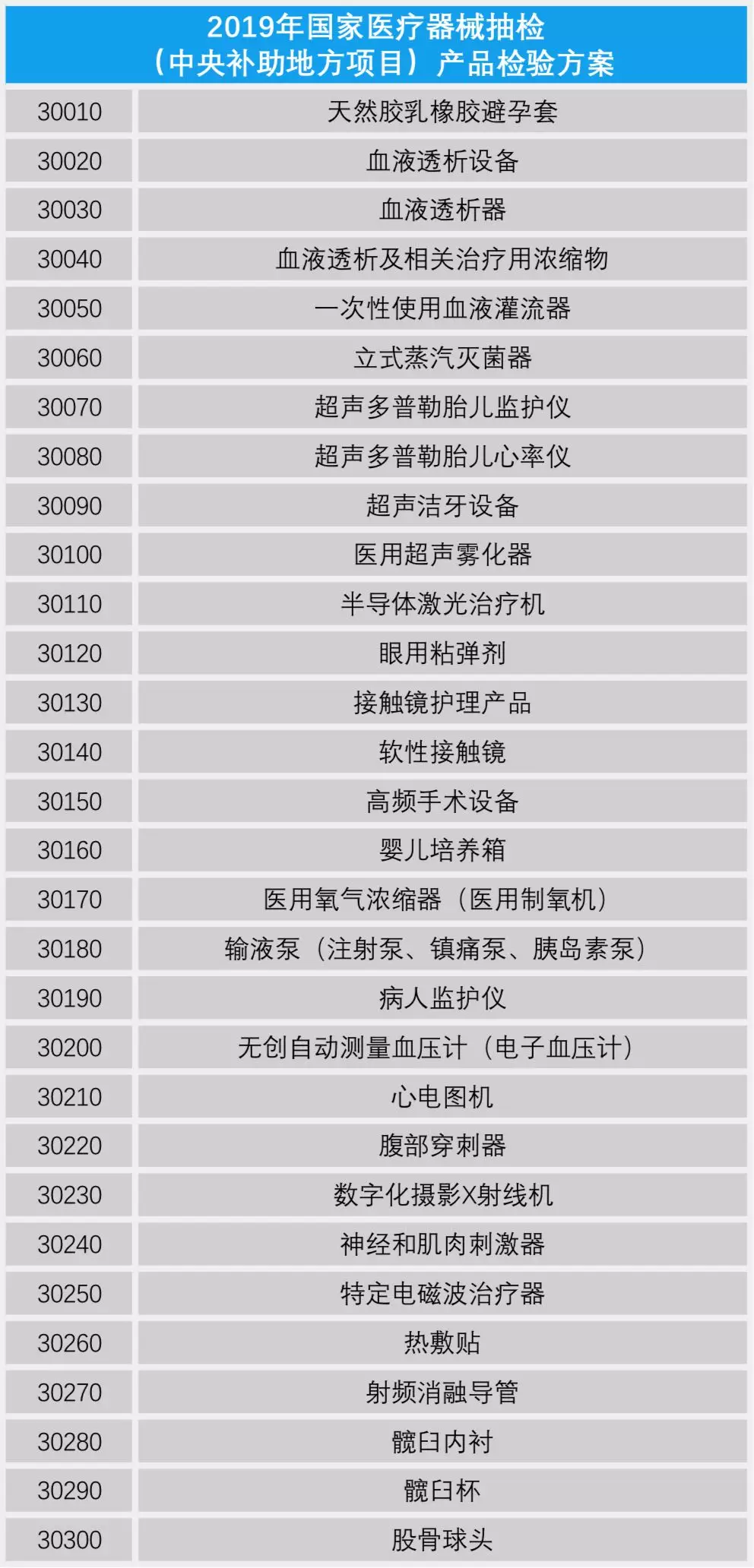
國(guó)家藥監(jiān)局在《通知》中要求�����,各省自治區(qū)直轄市藥監(jiān)局要按照《2019年國(guó)家醫(yī)療器械抽檢(中央補(bǔ)助地方項(xiàng)目)產(chǎn)品檢驗(yàn)方案》���、《2019年國(guó)家醫(yī)療器械抽檢(國(guó)家級(jí)預(yù)算項(xiàng)目)產(chǎn)品檢驗(yàn)方案》組織相關(guān)檢驗(yàn)機(jī)構(gòu)按醫(yī)療器械強(qiáng)制性標(biāo)準(zhǔn)以及經(jīng)醫(yī)療器械注冊(cè)或者備案的產(chǎn)品技術(shù)要求(注冊(cè)產(chǎn)品標(biāo)準(zhǔn))開展檢驗(yàn)工作。
證標(biāo)客整理了上述兩個(gè)產(chǎn)品檢驗(yàn)方案��,共計(jì)59類醫(yī)療器械產(chǎn)品列入抽檢范圍�����,包括中央補(bǔ)助地方項(xiàng)目中的病人監(jiān)護(hù)儀、心電圖機(jī)��、腹部穿刺器和血糖儀等49類產(chǎn)品�;以及國(guó)家級(jí)預(yù)算項(xiàng)目中的移動(dòng)式X射線機(jī)和多類檢測(cè)試劑盒等10類產(chǎn)品。(具體產(chǎn)品詳見下文)
對(duì)于產(chǎn)品抽檢項(xiàng)目的判定原則�,上述產(chǎn)品檢驗(yàn)方案顯示,所抽檢項(xiàng)目任意項(xiàng)判定為不合格�����,則本次抽檢綜合結(jié)論為不合格�。同時(shí),樣品在正常檢驗(yàn)過程中不能正常使用�����,本次抽檢綜合結(jié)論為不合格��。
產(chǎn)品抽檢旨在加強(qiáng)上市后醫(yī)療器械產(chǎn)品的質(zhì)量監(jiān)管�。據(jù)悉�����,2019年3月5日至7日,在廣州召開的2019年國(guó)家醫(yī)療器械抽檢工作座談會(huì)上�����,國(guó)家局醫(yī)療器械監(jiān)管司司長(zhǎng)王者雄表示�,國(guó)家醫(yī)療器械抽檢工作還存在各種問題和挑戰(zhàn),要求各單位精心組織����、整合全國(guó)醫(yī)療器械抽檢資源,規(guī)范行為���,狠抓嚴(yán)管����,做好不合格產(chǎn)品召回信息發(fā)布及工作總結(jié)的報(bào)送工作��。
此次國(guó)家藥監(jiān)局的抽檢工作通知中也明確了復(fù)檢工作以及推薦復(fù)檢機(jī)構(gòu)名單�����。
復(fù)檢工作上�,被抽樣單位或標(biāo)示生產(chǎn)企業(yè)(下簡(jiǎn)稱申請(qǐng)人)對(duì)檢驗(yàn)結(jié)論有異議的,可以自收到檢驗(yàn)報(bào)告之日起7個(gè)工作日內(nèi)向相應(yīng)的醫(yī)療器械檢驗(yàn)機(jī)構(gòu)提出復(fù)檢申請(qǐng)。為保證復(fù)檢效果���,申請(qǐng)人可以優(yōu)先從2019年國(guó)家醫(yī)療器械抽檢復(fù)檢機(jī)構(gòu)推薦名單中選擇����。復(fù)檢機(jī)構(gòu)應(yīng)及時(shí)受理復(fù)檢申請(qǐng)并開展檢驗(yàn)工作��。逾期未申請(qǐng)復(fù)檢的�,視為申請(qǐng)人認(rèn)可該檢驗(yàn)結(jié)果,檢驗(yàn)機(jī)構(gòu)不再受理復(fù)檢申請(qǐng)�。
同時(shí),在異議申訴上���,《通知》顯示���,被抽樣單位或標(biāo)示生產(chǎn)企業(yè)對(duì)檢驗(yàn)方法、判定依據(jù)等存在異議�,且無法通過復(fù)檢進(jìn)行驗(yàn)證的,應(yīng)當(dāng)自收到檢驗(yàn)報(bào)告之日起7個(gè)工作日內(nèi)�,向所在地省局提出異議申訴書面申請(qǐng),并提交相關(guān)證明材料����。
所在地省局應(yīng)當(dāng)在收到申請(qǐng)后2個(gè)工作日內(nèi),將異議申訴情況填報(bào)至國(guó)家醫(yī)療器械抽檢信息系統(tǒng),并在15個(gè)工作日內(nèi)進(jìn)行調(diào)查核實(shí)����、確認(rèn)核實(shí)結(jié)果�����,提出處理建議報(bào)中國(guó)食品藥品檢定研究院技術(shù)監(jiān)督中心����。相關(guān)省局未進(jìn)行調(diào)查審核、未提出核實(shí)結(jié)果和處理建議的的��,有關(guān)材料將予以退回�。逾期未提出異議或者未提供有效證明材料的,視為申請(qǐng)人認(rèn)可該檢驗(yàn)結(jié)果����。